O ensaio da vacina HIPRA inclúe dous hospitais da cadea HM que abriron unha bolsa de voluntarios
A farmacéutica biotecnológica Hipra anunciou a posta en marcha dun ensaio clínico para avaliar a inmunogenicidad e a seguridade dunha dose de reforzo coa súa vacina contra a Covid-19 en persoas vacinadas previamente con dúas dose da vacina de AstraZeneca.
Por Europa Press / Redacción | SANTIAGO DE COMPOSTELA | 07/03/2022 | Actualizada ás 18:53
O ensaio clínico da vacina contra a Covid-19 da farmacéutica HIPRA contará por primeira vez coa participación de dous hospitais galegos, o HM Modelo da Coruña e o HM Rosaleda de Santiago, que abriron unha bolsa de voluntarios para participar no estudo.
O ensaio clínico realizarase para avaliar a inmunoxenicidade e a seguridade dunha vacinación de reforzo coa vacina de HIPRA en persoas vacinadas previamente con dúas dose da vacina de adenovirus AstraZeneca. Este ensaio servirá para completar os resultados que a vacina de HIPRA obtivo ata o momento e, por primeira vez, participarán dous centros hospitalarios de Galicia.
Estes dous hospitais abriron unha bolsa para inscrición de voluntarios neste estudo, que empezará cando se reciba a aprobación por parte da Axencia Española de Medicamentos e Produtos Sanitarios, e o Comité Ético de Investigación con Medicamentos de HM Hospitais. Así, está prevista a aprobación para este mes de marzo.
Neste novo estudo participarán unhas 270 persoas maiores de 18 anos, para continuar avaliando a seguridade e eficacia das doses de reforzo de HIPRA contra a Covid-19, e compararase a resposta coa xerada por un vacúa control de mRNA (Pfizer-Biontech), despois de recibir unha vacina de adenovirus (Astrazeneca).
Ás persoas voluntarias que participen realizaráselles un seguimento de 6 meses para avaliar a seguridade a longo prazo e a resposta inmunológica. Para poder formar parte do ensaio, os voluntarios deben recibir dúas dose de Astrazeneca, como mínimo hai 3 meses, e non poden pasar a Covid-19.
Ademais dos centros hospitalarios de Galicia, tamén participarán neste proceso os hospitais universitarios HM Sanchinarro e HM Porta do Sur, e o Gregorio Marañón.
A vacina de HIPRA é un preparado de proteína recombinante adyuvada, baseada nun heterodímero de fusión do dominio de unión ao receptor (RBD) que contén as variantes B.1.1.7 (alfa) e B.1.351 (beta) do SARS-CoV-2. A vacina consérvase a temperatura de refrixerador (entre 2 e 8 ºC), o que facilita o almacenamento e distribución.
Ademais, a tecnoloxía utilizada permite unha gran versatilidade para adaptala a novas variantes do virus, se fose necesario no futuro. Os resultados obtidos a data de hoxe, demostran que a vacina produce anticorpos neutralizantes fronte ás VOC (variantes de "preocupación") actuais e tamén eficacia na prevención da enfermidade.
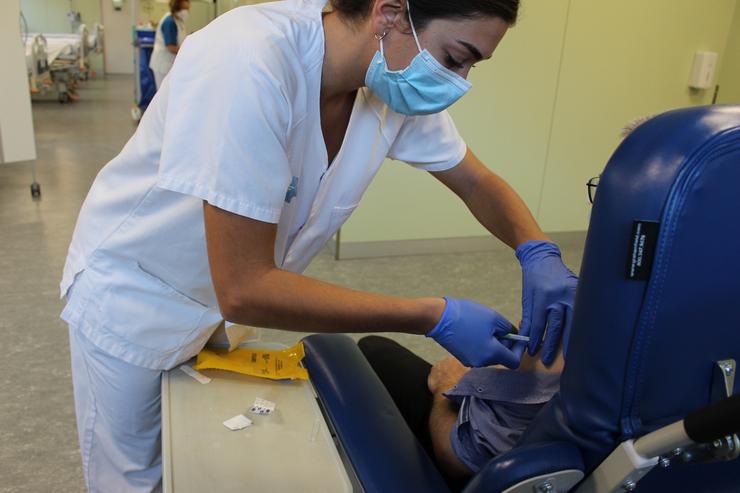
ENSAIO CLÍNICO
A farmacéutica biotecnológica Hipra anunciou a posta en marcha dun ensaio clínico para avaliar a inmunogenicidad e a seguridade dunha dose de reforzo coa súa vacina contra a Covid-19 en persoas vacinadas previamente con dúas dose da vacina de AstraZeneca.
Neste ensaio, que servirá para completar os resultados que a vacina de Hipra obtivo ata o momento, participarán cinco hospitais españois: os hospitais universitarios HM Sanchinarro e HM Porta do Sur, o Gregorio Marañón, HM Modelo e HM Rosaleda.
Os cinco centros abriron unha bolsa de persoas voluntarias para participar no ensaio que empezará unha vez recíbase a aprobación por parte da Axencia Española de Medicamentos e Produtos Sanitarios (AEMPS) e o Comité Ético de Investigación con Medicamentos de HM Hospitais. Prevese que a aprobación se dea a principios de marzo e procederase rapidamente ao comezo do ensaio.
Neste novo estudo, no cal participarán unhas 270 persoas maiores de 18 anos, continuarase avaliando a seguridade, tolerabilidad e a eficacia da dose de reforzo da vacina de Hipra contra a Covid-19 nun grupo de vacinados con dúas dose de AstraZeneca, e compararase a resposta que xera a dose de reforzo con Hipra fronte á que xera Pfizer-Biontech despois dunha vacina de adenovirus, como é Astrazeneca. Ás persoas voluntarias realizaráselles un seguimento de 6 meses para avaliar a seguridade a longo prazo e a resposta inmunológica.
As persoas que queiran participar no ensaio deben recibir dúas dose de AstraZeneca, como mínimo hai 3 meses, e non deben de pasar a Covid-19. Cada hospital habilitou un espazo na súa web para que as persoas interesadas poidan inscribirse. Unha vez o estudo estea aprobado, contactaráselles para proceder.
A vacina contra a Covid-19 que está a desenvolver Hipra é unha vacina de proteína recombinante adyuvada, baseada nun heterodímero de fusión do dominio de unión ao receptor (RBD) que contén as variantes B.1.1.7 (alfa) e B.1.351 (beta) do SARS-CoV-2.
Consérvase a temperatura de refrixerador (entre 2 e 8 ºC), facilitando o almacenamento e distribución. Con todo, a tecnoloxía utilizada permite unha gran versatilidade para adaptala a novas variantes do virus, se fose necesario no futuro. Os resultados obtidos ata o momento demostran que a vacina produce anticorpos neutralizantes fronte ás variantes de preocupación actuais e tamén eficacia na prevención da enfermidade.
Problemas cos comentarios?
Se tes problemas ou suxestións escribe a webmaster@galiciaconfidencial.com indicando: sistema operativo, navegador (e versións).
Agradecemos a túa colaboración.
- Catro evacuados tras a saída de vía dun coche en Carnota
- Primeira reunión entre a Consellería de Cultura e o director de Icomos
- Un barco de recreo pide axuda ante a dificultade para atracar en Muros
- Un motorista de 33 anos morre no Rosal arrolado por un vehículo cuxo condutor está en paradoiro descoñecido
- Morre unha muller en Ribadeo mentres practicaba mergullo
- Todo preparado en Nigrán para a cita forte do verán: o Reggaeton Beach Festival desembarca os días 26 y 27 de xullo















